Studienzentrum
Das Team des EB-Studienzentrums widmet sich intensiv der Feststellung von Wirksamkeit, Verträglichkeit und Sicherheit neuer Therapieansätze für EB. Das Ziel dieser aufwendigen Prüfungen ist die Marktzulassung einer wirksamen und sicheren neuen Therapie.
Klinische Studien ermöglichen PatientInnen den Zugang zu innovativen Behandlungsmöglichkeiten schon vor deren Zulassung und gewährleisten auf vielfältige Weise medizinischen Fortschritt. Für die Durchführung von klinischen Studien benötigt es ein Team aus ÄrztInnen, PflegerInnen und StudienkoordinatorInnen, welches für die wissenschaftliche Bewertung der Relevanz der Studie, die medizinische Betreuung der PatientInnen und die Regelung und Einhaltung organisatorischer Abläufe sowie bürokratischer und rechtlicher Vorgaben Sorge trägt.
Darüber hinaus ist die fachlich fundierte, strukturierte und empathische PatientInnenbetreuung während der gesamten Studienzeit wichtig. PatientInnen, die sich bereit erklären an einer Studie mitzuwirken und Teil einer neuen Entwicklung zu werden, sollen sich bestens betreut und über studienrelevante Abläufe bestens informiert fühlen.
Das EB-Haus Austria führt sowohl akademische Eigenstudien (Umsetzung hauseigener Forschungsergebnisse) als auch Sponsorstudien (durch Pharmafirmen an uns herangetragen) durch.
Durchführung klinischer Studien
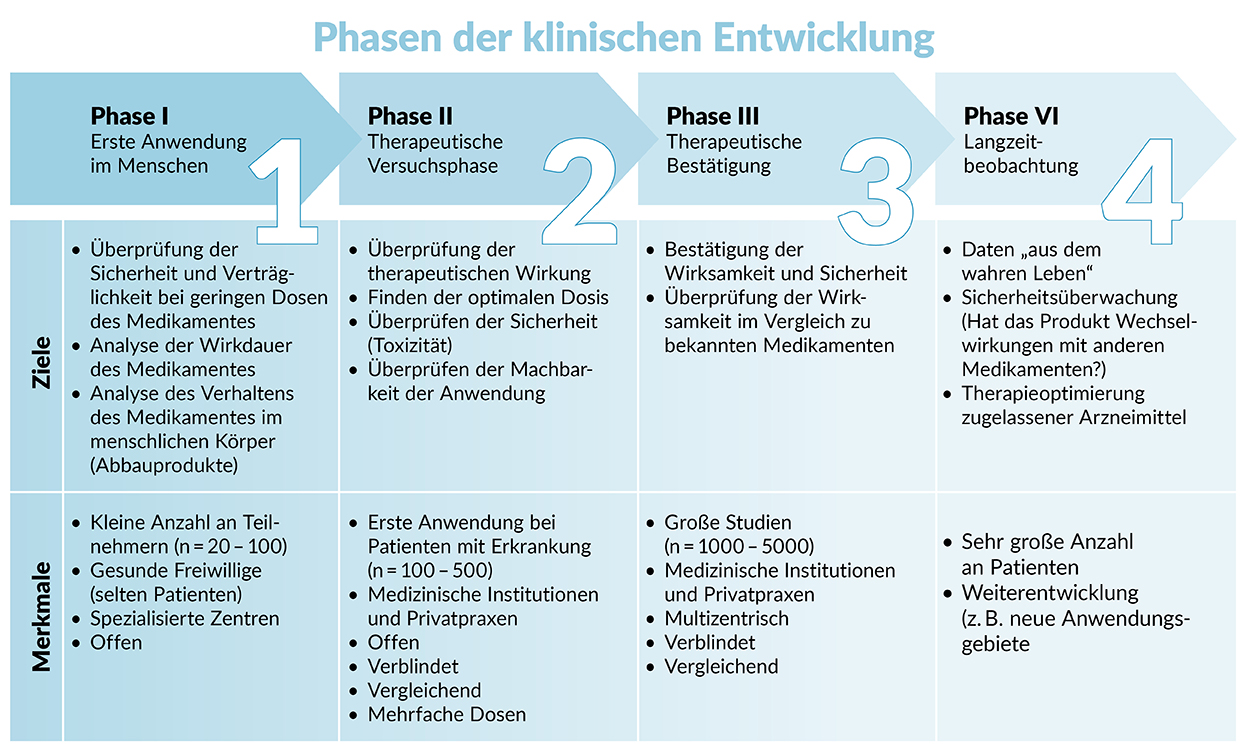
Die klinische Prüfung von Arzneimitteln durchläuft normalerweise Testungen in drei Phasen (siehe Abbildung). Da es sich bei EB aber um eine seltene Erkrankung handelt und somit nicht für alle Phasen genügend Betroffene teilnehmen können, dürfen die Phasen I + II häufig zusammengelegt werden.
Ausgangspunkt für eine Prüfung an PatientInnen ist immer eine fundierte wissenschaftliche Vorarbeit im Labor. Die dort erlangten Ergebnisse müssen zusammengefasst und eine detaillierte Aufstellung der geplanten Studie (Studienprotokoll) erstellt werden. Gemeinsam mit Antragsformularen, PatientInneneinverständniserklärungen und Qualifizierungsunterlagen aller beteiligten Personen werden diese bei Behörden und Ethikkommissionen zur Beurteilung eingereicht. Erst nach deren Zustimmung ist eine Umsetzung möglich.
Die Auswahl der EB-Betroffenen erfolgt nach strikten Vorgaben (Ein- und Ausschlusskriterien), welche durch das Studienprotokoll vorgegeben werden. Aufgrund des engen Kontaktes zu unseren PatientInnen und das oft sehr detaillierte Wissen um deren Krankengeschichte kann hier bereits durch das Studienteam eine Vorauswahl getroffen werden. Es werden dann jene PatientInnen kontaktiert, deren Profil für eine Teilnahme passend wäre. Die Entscheidung für oder gegen eine Teilnahme liegt aber letztlich immer beim Patienten/bei der Patientin.
Während der Durchführung der klinischen Studie ist eine akkurate Dokumentation wichtig. Diese erleichtert die Auswertung der erhaltenen Studiendaten und muss behördlichen Vorgaben Genüge tragen. Die Einhaltung aller, im Studienprotokoll festgelegten Abläufe und Tests, wird regelmäßig von Extern durch Mitarbeiter einer CRO (Contract Research Organization) überprüft.
Nach der Beendigung der Studie werden die Daten statistisch ausgewertet, nach Möglichkeit in Fachjournalen publiziert und das weitere Vorgehen bewertet (Wiederholung der Studie mit veränderten Parametern; Weiterführende Studie zur Bestätigung der Wirksamkeit; Anstreben einer Marktzulassung).